CNAS+国家CMA二合一扩项现场评审
2022/07/06

演讲 一 相容性常见发补案例分享

简介:微谱相容性研究中心技术总监——杨潇军先生,曾参与国家药审中心《弹性体相容性指导原则》的起草,萃取物及溶出物年会中国区专家组成员,微谱相容性研究技术带头人。曾先后为国内1000余家制药企业3000多个药品研发项目提供相容性研究服务。
尊敬的各位领导、各位专家以及各位业界同仁们,大家上午好。很高兴今天作为第一位分享嘉宾,与大家分享交流。今天也是借这个机会与大家分享一些在实际工作中遇到的案例。我今天分享的内容大概分三方面:第一,相容性背景介绍。第二,案例分享。第三,案例总结。

我先讲第一部分相容性背景。一个药品从生产到最终使用过程当中会经历这么一个阶段:原料药容器生产(玻璃体)、生产组件、生物医药(一次性使用系统)、成品包装、给药器具(注射器、留置针),从研发到使用到的多多少少都会进入药品当中,我们是基于整个生物线进行传递。相容性板块大概分三块:一是包装材料,二是工艺组件相容性,三是给药器具相容性。
我把三块总结一下:第一,GLP阶段,包含了可提取物研究和初步毒理评估。第二,GMP阶段,包含了方法学验证、浸出物测试、最终安全性评价。总体来讲,我认为前端的技术研究偏GLP研究,更多是研究、风险评估、数学分析。后端是偏GMP阶段,制定标准、做企业方法学等。
基于这么一个阶段,我把整个市场上包括我遇到的、客户给到我们的一些研究报告,简要分成了三类:(一)糟糕类。仅采用药液提取、提取方式单一、未明确AET、采用低专属性的HPLC设备、无毒理评估、通用验证(一套验证吃天下)、目标物固定N个。(二)一般类。做法有一定的科学性,但至少在目前阶段,在法规要求是越来越严格的,因为对安全性要求越来越高了。比如,药液加减PH值、提取方式固定模式、不够严格的AET、采用LC-MS(DAD)、GC-MS等设备、毒理评估数据来源不是很全、验证不够全面、目标物制定逻辑不清楚。(三)优秀类。我们选择要全面,要有合理性,其次设备硬件要得到满足。比如说,采用了UPLC-MS、SM、GC-MS等辅助定性。我们的毒理评估方法要合理,数据检索要全面,验证要满足ICH Q2,该做的项目、精密度等工作都需要做。最后,我们还要将目标物要按指导原则含量高、毒理强进行制定。
下面,进入第二部分,我讲一些案例分享。
第一个案例,未对弹性体中特殊关注的物质进行考察。我们的主要配方是溴化丁基橡胶,它的主要作用是主体胶,钛白粉具有着色作用,炭黑具有着色、补强作用,高岭土和滑石粉具有填充作用,活性氧化镁具有活化作用,硫磺和氧化锌具有硫化作用,而凡士林和硬脂酸具有助剂作用。
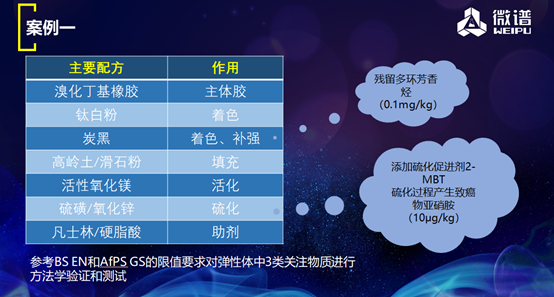
像炭黑多多少少都有残留多环芳香烃,又因为橡胶有一个硫化过程,所以会产生致癌物亚硝胺。大家也要了解一些,为什么弹性体对这两种东西比较特殊?因为是自然的、明确的,所以要特别关注。针对这种特别关注的,大家要参考BSEN和AfPS GS的限值要求,在弹性体中三类关注物质进行方法学验证和测试。这是针对于婴儿奶瓶和奶嘴的限制,这个不能直接用于药品的,我们是需要进行计算的。
第二个案例,未对包材中的抗氧剂的降解产物进行研究。以前,我们做研究时经常会发现330、1010等抗氧剂,特别是168有一个辅助抗氧剂的作用,主要抗氧剂被氧化之前先被氧化掉。我们要了解整个抗氧剂过程中产生的物质,这个BHT(音)图,它在整个占比过程当中会出现两种物质,要重点关注。我的建议是要了解清楚降解产物反应机理,基于降解产物原理和目标建立材质相关的可提取物和浸出物数据库。

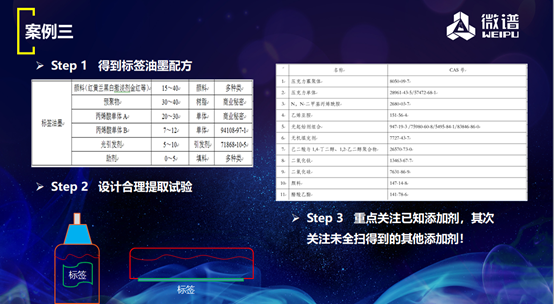
第三个案例,未对标签、油墨(特别关注甲苯)和粘合剂中的浸出物进行研究。在遇到这类案例之前,我们不能很着急去做研究。第一步,要得到标签油墨配方。右边这个图是非常不错的油墨配方表,知道了这些配料之后就可以设计实验了。第二步,设计合理提取试验。在瓶子上面贴满标签,涂满油墨,这也是一种方法。或者是把标签贴在下面,在上面进行提取。第三步,重点关注已知添加剂,明确讲到的添加剂都要特别关注,像甲苯是非常值得关注的。其他的添加剂就要通过人工解析方式再去做解析。如果供应商不配合怎么办呢?在这种情况下,我们就把油墨做一个成分分析,来得到里面的添加剂信息,这也是一个很好的办法。
第四个案例,结合ICH Q3D的要求,通过科学和基于风险评估原辅包、生产设备中可能引入的元素杂质。这里我们分两个点来了解:一是药品或者辅药里面是不是有一些杂质,在做研究的时候没有加入;二是生产设备中是不是有被忽略的杂质。
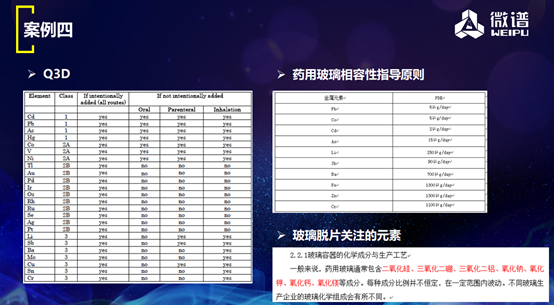
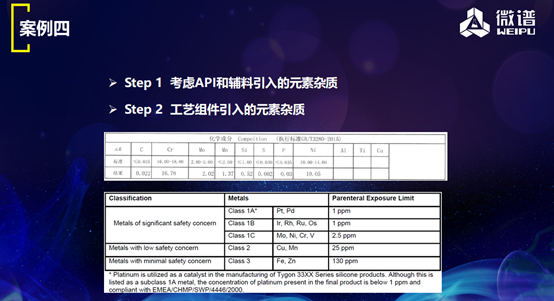
我们根据元素做了不同分类,做了玻璃脱片研究。我认为药企首先要考虑API和辅料引入的元素杂质。其次,要考虑工艺组件引入的元素杂质,比如说不锈钢组件,这些组件一定要配方列表,这两张图上面是不锈钢管,下面是硅胶管,里面就提到了有残留物,这些都要进行研究。
我们还要确定需要研究的元素,这里面又有几个小问题。比如说,要不要考虑Na、K、Ca和Mg呢?又比如说,未明确PDE的元素怎么制定限值呢?如果找不到的话,可以按照风险元素进行整改。风险元素注射多了会得老年痴呆,对于大容量的注射剂要求是有规定的。再比如说,2L的输液怎么考虑限值?
第五个案例,对玻璃内表面脱片进行研究。这里面有两种情况:一种情况是客户做了部分研究,一种情况是对脱片直接进行全部研究。这里先给大家介绍一下玻璃脱片考虑的是什么。我们先了解一下典型的管制品,像图中的尖部和底部会进行二次受热,玻管在加热过程当中会经受上千度的高温,在高温过程当中二氧化硅会沸腾,沸腾就会起泡,起泡就会在表面生成一个一个小圈,这是固有的缺陷。
其次,我们来了解一下亚甲基蓝染色法。我们平时在清洗的时候是摇一摇,这是洗不掉的。所以,我们认为场发射电子显微镜法是最合理的。
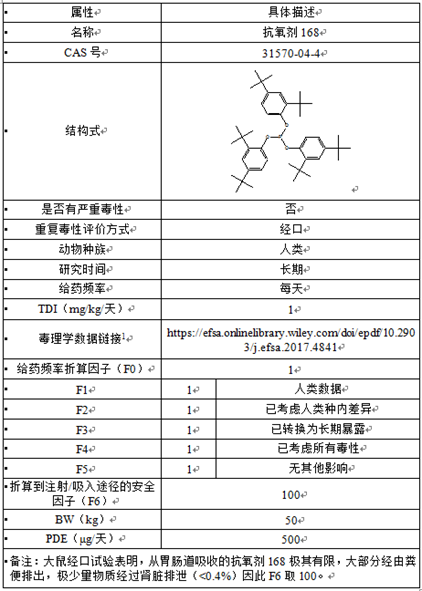
第六个案例,请提供某化合物的毒理学数据来源。这是一个抗氧剂168的降解产物三磷酸脂的评估案例,这是2014年的一篇文献,这是我们做的链接,我们对里面的取值进行了评估和预测。这是我们常用的一些东西,里面很多都是免费的。我们发现很多他们是没有找到合适的方法和手段,就导致很多问题无法解决。
第七个案例,本品处方中含40%的丙二醇、20%的山梨醇,请参考弹性体指导原则对胶塞中的添加剂进行提取试验。我的产品当中如果原提取液是20%的乙醇,就不能涵盖产品的特性。如果用1%吐温去提的话,相当于50%的乙醇,像提取的因素是非常关键的,比如说溶液组成、接触方式(倒置、充分接触组件)、温度时间(考虑药品在实际生产、在储存、使用过程当中的变化)。基于前面的试验,我们首先提取了出了“酸碱醇”,这是比较相对严苛的提取物液中找到的目标物。其次,我们提取了模拟液确认目标物。最后,我们去做浸出物。

第八个案例,请提供浸出物制定的依据。这个方案,整体元素有初步依据的,有机物整个研究方案未写明如何制定。这是一篇CDE原文,明确提到了重点关注检出量较大、检测灵敏度低的物质。这是一篇弹性体指导原则原文,明确提到了安全指数的情况。这是有一些指数概念,像氯化苄,这是毒性最强的,就用它做化合物研究。这是一个相对合理的评估方式。
第九个案例,请提供硅胶管的材质证明文件,同时参考USP665、1665对硅胶管进行评估,基于风险考虑是否需要进一步完善组件系统整合。这两张图说明了是做了细胞活性,是做过有生物相容性试验的。
首先,我们根据USP665、1665进行风险评估,在相同性点上测试是进行了提取物测试实验。其次,我们根据BPOG进行风险评估。看到底处于上游、中游还是下游阶段,它的测试量与我们是保持一致的。最后,根据不同设备进行检测。比较推荐的是NIST数据库进行支持。
第十个案例,请提供硅胶管重复使用的证明文件。这个案例是最近遇到最多的案例,这是企业的痛点问题,我们也与企业沟通过了。(1)特殊硅胶管价格高。(2)生产过程中清晰灭菌+生产流程较长。最后,我们也达成了两个共识:(1)灭菌过程对硅胶管影响极大。(2)无法在产线上实现。我们的建议是合并灭菌过程,加速模拟实际硅胶管使用情况,然后再进行检测。
第十一个案例,未对临床实际使用中的给药器具(注射器、输液管路)等进行相容性研究。我们明确了药品的临床使用方式。比如说,在皮下注射静脉推注肌肉注射、短时间内静脉滴注、长时间静脉滴注。
第十二个案例,研究的材质和供应商过少。这个问题要先理解一下,前面提到了给药器具有很多,材质少、供应商是指什么少呢?我们要看一下这些材质的情况。(1)对于一次性使用无菌注射器,通常会有带针的情况,会有给针的规格。其次,规格是否符合复溶体积的要求,或者是常见PP材质。(2)一次性使用输液器。像有带针、不带针,或者有带过滤器及孔径的,常见的有PVC、TPU、TPE材质等,其中典型的PVC含有30增塑剂,这是最需要关注的。(3)留置针。常见的是聚氨酯材质。
PVC材质是传统的材质,大部分含有DEHP增塑剂、粘合剂环己酮等。它对亲酯性药品有不相容性,像紫杉醇等。TPU材质是新型材质,通常含有TOTM或类似的增塑剂、粘合剂环己酮。TPE材质是新型材质,通常含有粘合剂环己酮等。我们建议是:至少对输液选择两个材质,这样就可以对应两个厂家,也就可以满足要求了。
第十三个案例,我们看一下怎么去取得做配伍液。这个案例主要考虑配伍禁忌、再考虑实际使用情况、选择配伍液,最后根据配伍液的情况选择合适的包材材料。配伍液的包装材料要不要考虑相容性呢?我跟注射器厂家有沟通过,他们一批可能挣不多少钱。很多注射器是不稳定的,所以材质就不会稳定。而对于包装材料来说,材质是比较干净而稳定的,相对来讲它更可靠一些。我们的建议是:在选材时说明原因,但不用考察相容性,在配伍液中寻找稳定性。
第十四个案例,原研说明书。配伍浓度在1毫克到5毫克之间,我们通常用输液器与自制品参比制剂进行相容性考察。建议是最高和最低浓度和配伍方式,考虑2种配伍方式下浸出物的进出情况,主要考虑对比。
第十五个案例,未对输液器中明确添加的增塑剂进行研究。针对这种案例,我们在试验前分析确认清楚给药器具中的添加剂信息,要先了解材料,如果不了解材料就做实验一定会有问题。
第十六个案例,未进行配伍稳定性研究和未进行吸附研究。我大概把整个配伍稳定性分了理化性质变化、含量杂质变化(是否有降解、葡萄糖中糠醛)、储存条件(冷藏、室温、避光)、其他(配伍浓度放置方式)。这是一个吸附案例,我们建议:一是多时间取样,建议至少5个时间点;二是取样部位(针头处);三是空白对照,吸附后看对照趋势;四是含量的变化趋势,并不是去看含量是否跟我的标准对应。
第十七个案例,上半个月自己研究过程中遇到的案例,我认为很典型,也想与大家分享一下。这是DEHP的检测量变化情况,我们在做第一次是13.58套,做第一次复测时是5.54,第二次复测是18.25。我们又在不同温度下进行了测试,后来发现确实是因为温度原因造成的不一样。以上大概是所有发布案例我做了汇总。
第三部分,我做一个总结,很多企业都有难点,比如说行业领域现状,像硬件软件投入大、监管难、材质复杂、专业性强、鱼龙混杂(很多企业不知道自己做,还是选择外包机构,选择外包机构又不知道如何选择)。我们如何破呢?就要做出优秀的点。我认为可以用POEM来实现。